實(shí)施優(yōu)先審批的醫(yī)療器械范圍為:一是診斷或治療罕見(jiàn)病、惡性腫瘤且具有明顯臨床優(yōu)勢(shì)的醫(yī)療器械、診斷或治療老年人特有和多發(fā)疾病且目前尚無(wú)有效診斷或治療手段的醫(yī)療器械、專用于兒童且具有明顯臨床優(yōu)勢(shì)的醫(yī)療器械、臨床急需且在我國(guó)尚無(wú)同品種產(chǎn)品獲準(zhǔn)注冊(cè)的醫(yī)療器械。二是列入國(guó)家科技重大專項(xiàng)或國(guó)家重點(diǎn)研發(fā)計(jì)劃的醫(yī)療器械。
關(guān)于我們 ∨
OLABS ∨
奧咨達(dá)OLABS
全球性的創(chuàng)新型醫(yī)療器械專業(yè)孵化加速器,位于中國(guó)多個(gè)醫(yī)療器械產(chǎn)業(yè)中心的核心地帶,通過(guò)醫(yī)療器械全鏈條技術(shù)服務(wù)體系、專業(yè)共享軟硬件平臺(tái)和醫(yī)械數(shù)字化支持......
解決方案 ∨
解決方案
全方位的醫(yī)療器械服務(wù)和解決方案,支持從專利到研發(fā)再到臨床注冊(cè)的各類創(chuàng)新無(wú)源醫(yī)療器械產(chǎn)品轉(zhuǎn)化,打造高能級(jí)醫(yī)療器械專業(yè)孵化器,提供醫(yī)療器械全鏈條、全方位、專業(yè)化孵化服務(wù),解決醫(yī)械成果轉(zhuǎn)化與初創(chuàng)企業(yè)孵化全過(guò)程加速需求。
聯(lián)系方式 ∨


 更多
更多 收起
收起
先審批.jpg)
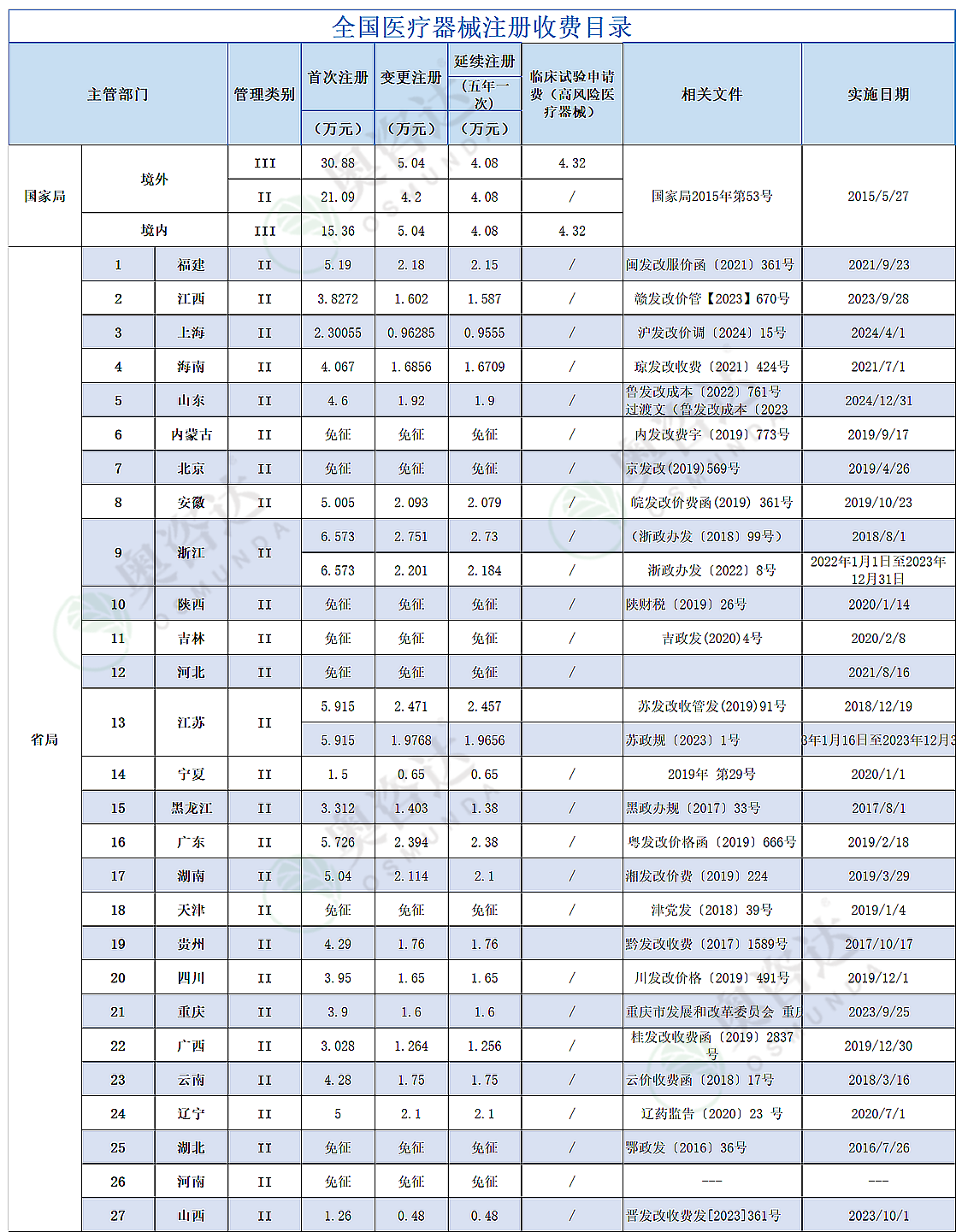 單位:萬(wàn)元
單位:萬(wàn)元
